G. Clergeau, S. Nadeau, D. Denis, A. Péchereau
L’examen de la réfraction chez l’enfant strabique pose le problème du manque de coopération de ces derniers et de la difficulté à interpréter les examens subjectifs. Or, chez les enfants, il est primordial d’obtenir une réfraction de qualité qui permettra de corriger les amétropies et de lutter contre l’amblyopie et la part réfractive du strabisme.
Ces constatations expliquent le recours à des examens paracliniques « objectifs » permettant une meilleure évaluation de la réfraction.
L’outil historique à notre disposition pour évaluer de façon objective la réfraction est la skiascopie. Cette technique, découverte en 1873 par l’ophtalmologue français Cuignet [15] et perfectionnée par Parent, s’est répandue par la suite dans les pays anglo-saxons grâce à l’invention du skiascope en fente par Copeland en 1926. La skiascopie a été particulièrement utile pour une estimation de la réfraction chez les patients dont la coopération était difficile à obtenir.
Le principe de la skiascopie est d’observer le mouvement d’une aire du fond d’œil qui s’illumine grâce à la lumière du skiascope. L’ajout de lentilles d’essai devant l’œil va modifier le mouvement apparent de l’aire illuminée. Si cette aire présente un mouvement de même sens que le mouvement du skiascope, on ajoute des lentilles positives ; si elle présente un mouvement en sens inverse, on ajoute des lentilles négatives. La lentille qui produit l’inversion du mouvement détermine le degré d’amétropie.
Cette technique, fiable et reproductible chez un opérateur entraîné, donne des résultats plus aléatoires chez les utilisateurs moins expérimentés. Elle nécessite en outre une certaine fixation du patient donc une coopération, et est relativement longue à réaliser.
Ces inconvénients ont été supprimés par l’avènement des réfractomètres automatiques fixes ou portables.
Son principe [1, 18, 46] repose sur :
-
la rétinoscopie (principe de l’optomètre) : déplacement d’une cible lumineuse derrière une lentille pour déterminer le point de neutralisation des rayons émergents de l’œil, donc son degré d’amétropie ;
-
le principe de Scheiner : déplacement d’une cible lumineuse pour faire converger sur la rétine deux faisceaux lumineux en un seul.
La rétine maculaire est alignée sur une cible que le patient doit fixer (montgolfière, etc.). L’appareil éclaire la rétine par un faisceau infrarouge (l’utilisation de lumière hors du spectre visible limite le phénomène d’accommodation) au travers de fentes lumineuses, animées de mouvements de rotation. Un système automatique de brouillage va également limiter l’accommodation et permettre de réaliser une mesure sur un œil « au repos ».
L’analyse est effectuée par deux photorécepteurs A et B. La distance entre les deux étant fixe, l’appareil mesure l’intervalle de temps qui sépare la stimulation successive de ces deux photorécepteurs et en déduit l’amétropie dans tous les méridiens sur 360°.
Les avantages de la réfractométrie automatique (fig. 4-1) sont :
-
la rapidité : 0,3 seconde par mesure ;
-
la précision : calculs à 0,25 d voire 0,12 d près ;
-
la fiabilité et la reproductibilité des calculs ;
-
la large gamme de mesures permises : de – 18 d à + 23 d pour la sphère et de – 10 d à + 10 d pour le cylindre ;
-
la possibilité que la mesure soit réalisée par une personne autre que l’ophtalmologiste, permettant un gain de temps lors de la consultation.
Les limites de ces appareils sont :
-
la non-suppression de l’accommodation (nécessité d’une cycloplégie) ;
-
la difficulté de réalisation en cas de mouvements oculaires : enfants de moins de deux ans, nystagmus, patients infirmes, etc. ;
-
l’existence de troubles des milieux transparents.
Pour rendre possible l’utilisation des réfractomètres automatiques dans le plus grand nombre possible de situations, des réfractomètres automatiques portables ont été développés.
Il en existe plusieurs modèles (Retinomax 3 de Nikon, ARK-30 de Nidek, etc.) dont les caractéristiques sont proches [10, 11, 14, 28, 29, 34, 37].
Ses principaux attraits par rapport aux réfractomètres automatiques fixes sont (fig. 4-2) :
-
une cible attrayante à regarder, permettant d’éveiller l’intérêt de l’enfant dans le cadre d’une utilisation en pédiatrie ;
-
la présence d’un seul appui (frontal) pour le patient, voire pas d’appui, avec absence de contention de la tête (moins effrayant pour les enfants) ;
-
son caractère transportable (son poids est inférieur à 1 kg), le rendant utilisable dans plusieurs positions ; cette caractéristique le rend particulièrement utile pour une utilisation au bloc opératoire ou en ambulatoire chez des patients peu mobilisables.
Il existe deux modes d’utilisation :
-
un mode « Normal », correspondant à celui d’un réfractomètre fixe (une mesure en 0,34 seconde) et utilisant une méthode de brouillage qui minimise l’accommodation (donc la myopie instrumentale) ;
-
un mode « Quick », permettant des mesures immédiates (0,07 seconde), particulièrement utile en cas de mouvements oculaires ou chez l’enfant agité.
L’utilisation de ces appareils est aisée même si elle nécessite quelques précautions : il est nécessaire de bien aligner l’appareil dans les trois plans de l’espace (horizontal, vertical et torsionnel) ; un diamètre pupillaire minimal de 2,3 mm est requis.
La lecture du résultat doit de faire après vérification de l’indice de fiabilité de chaque mesure (idéalement au moins 7) et élimination des mesures aberrantes (liées à des mesures prises en l’absence de fixation). La valeur « représentative » sélectionnée par l’appareil correspond à la médiane des mesures pour chacune des valeurs réfractives.
Les limites des réfractomètres automatiques portables sont :
-
une surévaluation de l’astigmatisme en cas d’amétropie forte ;
-
un risque d’erreur de latéralisation (celle-ci se faisant normalement automatiquement) ;
-
une imprécision sur l’axe de l’astigmatisme, particulièrement si l’appareil est mal positionné.
L’efficacité des réfractomètres automatiques portables, sous cycloplégique, est comparable aux réfractomètres automatiques fixes et à la skiascopie.
Plus pratiques d’utilisation et moins encombrants qu’une boîte de verre d’essai accompagnée de sa monture, les réfracteurs automatiques (fig. 4-3) ont vu leur utilisation se répandre largement.
Ses intérêts sont :
-
une mesure plus rapide de l’acuité visuelle subjective chez le grand enfant et l’adulte ;
-
une réalisation facile et rapide de la méthode du « brouillard » lorsqu’une cycloplégie n’est pas indispensable ;
-
une connexion aux autres appareils d’examen (réfractomètres notamment) ;
-
un gain de temps par l’absence de manipulation des verres.
Cet appareil permet également une utilisation plus aisée de certains tests. Ainsi, l’utilisation du cylindre croisé de Jackson permettra d’affiner l’axe et la puissance du cylindre avec moins de risque d’erreur que lors de sa réalisation « manuelle ». De même, l’utilisation des prismes, des verres polarisés et du test rouge-vert est simplifiée.
Il existe des limites inhérentes à ces appareils :
-
la difficulté à voir les yeux du patient, entraînant une certaine perte du contact, une difficulté à observer son comportement (plissement des yeux ?) et la nécessité de surveiller le positionnement de la tête et des yeux du patient ;
-
l’examen de la vision de près est plus difficile qu’avec une monture d’essai, particulièrement chez les enfants ou les sujets âgés (position non « physiologique » du test de Parinaud).
Les cycloplégiques sont traités plus loin dans ce chapitre. Ici nous voudrions souligner quelques aspects quant à leur intérêt dans la réfraction. Nous nous limiterons aux deux seuls cycloplégiques vraiment efficaces, l’atropine et le cyclopentolate.
Dans un souci d’absolu qui sert à la fois de raison et d’excuse, on entend que nombre de nos collègues préfèrent l’atropine au cyclopentolate. C’est clairement une erreur pour les raisons suivantes :
-
les perdus de vue : les études de la littérature qui ont inclus les perdus de vue (ce qui est la réalité de l’exercice quotidien) dans les comparaisons entre ces deux produits montrent toujours la supériorité du cyclopentolate (parce qu’il n’est pas nécessaire de faire revenir le patient) ;
-
l’âge : avec l’âge, la cycloplégie a toujours la même importance (jusqu’à cinquante ans) et ne peut plus être réalisée à l’atropine ;
-
la multiplication des cycloplégiques : c’est sûrement la meilleure façon de s’adapter à ce paramètre variable tant que l’enfant grandit ; imaginer qu’il faille faire une cycloplégie régulière (deux fois par an) à l’atropine à partir de six ans est le plus sûr moyen de n’en réaliser aucune ;
-
le port de la correction optique totale : c’est le plus sûr moyen de « faire dégorger l’hypermétropie » (A. Roth) à condition de multiplier les cycloplégies et de faire porter la correction optique totale.
Le cycloplégique d’action lente garde totalement sa place dans quelques situations particulières :
-
recherche d’une hypermétropie latente devant un petit angle qui ne serait plus chirurgical si une augmentation de la correction de l’hypermétropie permettait de lever un spasme accommodatif entraînant une convergence de quelques dioptries prismatiques ;
-
amblyopie résistant à la thérapeutique ;
-
enfants pigmentés, bien que cela ne soit pas toujours une évidence ;
-
difficultés d’examen.
La cycloplégie rapide est une véritable révolution dans la prise en charge de tous les patients présentant des troubles sensorimoteurs. Elle doit être utilisée larga manu. Le déremboursement de cette molécule est une grave erreur.
La dilatation est un outil remarquable pour affiner la réfraction subjective. En effet, le myosis permet d’augmenter la profondeur de champ, donc la tolérance à la défocalisation. La mydriase, en revanche, permet de limiter la profondeur de champ, donc d’affiner la réfraction subjective.
La cycloplégie et la mydriase vont donc toutes les deux dans le sens d’un raffinement de la réfraction. Il serait dommage de ne pas les utiliser.
Les appareils mis au point pour calculer l’implant dans la chirurgie de la cataracte (biomètre, kératomètre, IOLMaster®, Lenstar®, etc.) [35] sont de formidables adjuvants de toute prise en charge d’un trouble réfractif significatif. Ils permettent de décomposer les paramètres du trouble amétropique :
-
devant cette myopie, existe-t-il une augmentation de la longueur axiale ou une cornée très plate ? Le pronostic à long terme sera différent : dans le premier cas, cette myopie évoluera probablement ; dans le deuxième cas, elle sera probablement stable ;
-
cette hypermétropie forte est-elle due à un très petit œil, à une cornée très courbe ou à un mixte des deux ?
-
cette anisométropie est-elle réelle ou liée à un spasme accommodatif que la cycloplégie n’arrive pas à lever ?
-
chez cette adolescente qui passe son temps à lire, cette myopie qui évolue est-elle due à un spasme accommodatif ou à une augmentation de la longueur de l’œil (sachant que 1 mm correspond à 3 d) ?
Les paramètres biométriques en donnent les réponses.
Il est incontestable que paramètres biométriques sont une source d’informations précieuses dans la prise en charge des anomalies réfractives.
La détermination de la réfraction par les moyens cliniques et paracliniques évolue et évoluera de façon permanente et importante. Tous ces moyens permettent d’obtenir des réponses de plus en plus précises donc efficaces. Tous ces moyens sont un incontestable progrès dans la prise en charge des patients présentant des troubles sensorimoteurs.
Un sujet hypermétrope qui n’a pas spontanément une acuité normale a besoin pour y parvenir d’une certaine correction positive. Cette valeur est qualifiée d’hypermétropie obligatoire. La quantité de correction positive supplémentaire tolérée qui ne modifie pas l’acuité est qualifiée d’hypermétropie facultative. La somme de ces deux hypermétropies est qualifiée d’hypermétropie manifeste. Celle-ci est la valeur maximale qu’on peut obtenir à partir de l’examen subjectif [41]. Cependant, toute activité d’exploration visuelle, en particulier lorsqu’il existe une participation subjective de déchiffrage, va entraîner une réaction accommodative modifiant l’évaluation de la réfraction réelle qui est l’objet de la recherche. Par ailleurs, chez le nourrisson il n’y a pas d’examen subjectif.
Certaines méthodes ont été considérées comme permettant d’évaluer réellement cette réfraction manifeste. Cette dernière peut être obtenue chez le sujet coopérant en induisant une fixation dite à l’infini (à partir de 6 m) sur un optotype neutre et en réalisant une skiascopie sur l’œil controlatéral. Un résultat identique pourrait être obtenu chez le nourrisson en skiascopie dite de proximité (à 50 cm) dans une pièce sombre [30]. Même avec une relaxation optimale, ces méthodes laissent généralement persister ce qu’on dénomme un tonus accommodatif de base, appelé hypermétropie latente, qui est évalué à une valeur de + 0,75 d à + 1,25 d selon l’âge. En fait, les bilans réalisés sous cycloplégie montrent que cette hypermétropie est très variable et imprévisible. Si on ajoute que la conscience d’un objet proche peut induire une certaine accommodation, il apparaît évident que toute mesure non cycloplégique réalisée en skiascopie ou en autoréfractométrie ne peut comporter une relaxation fiable de l’accommodation. Les définitions réfractives et leur méthode d’analyse sont applicables à la myopie.
Une neutralisation de l’accommodation la plus complète possible apparaît donc indispensable pour révéler l’hypermétropie totale et gérer de façon correcte toute anomalie réfractive. Il est également important de souligner que si le souci accommodatif est majeur chez le jeune enfant, il persiste à des degrés divers jusqu’à l’évolution terminale de la presbytie. Une étude comparative de la correction subjective donnée à quarante ans puis à soixante ans a montré une augmentation hypermétropique relative moyenne de 1,10 d, mais avec des valeurs dépassant les 3 d. On constate une nette asymétrie entre la situation des hypermétropes et celle des myopes : pour les premiers, une augmentation ou une stabilité de l’hypermétropie est constatée dans 97 % des cas, alors qu’une diminution de la myopie n’est retrouvée que dans 30 % des cas. Ceci est un argument pour penser que l’explication ne réside pas dans une simple modification sénile du segment antérieur. Ces constats sont également valables pour les strabiques adultes avec, souvent, des conséquences fonctionnelles notables.
Une des fonctions essentielles à l’exploration de l’espace est représentée par l’accommodation. Celle-ci étant sollicitée en quasi-permanence, il existe rarement une relaxation suffisante pour pouvoir déterminer par le seul examen visuel la valeur de base de l’état réfractif. Cette donnée est pourtant essentielle dans l’établissement d’une correction optique adaptée. En conséquence, seule une paralysie de cette accommodation permet d’atteindre cet objectif. Cette action définit la cycloplégie.
Le mécanisme réflexe d’accommodation est sous la dépendance du système parasympathique dont les voies cheminent dans la IIIe paire. Le système parasympathique a pour médiateur l’acétylcholine qui est libérée au niveau des terminaisons nerveuses mais ne produit ses effets que lorsque la molécule est captée par des récepteurs muscariniques. Le principe commun à toutes les molécules cycloplégiques est de bloquer ces récepteurs muscariniques. Ces substances qualifiées de parasympathicolytiques sont donc plus précisément des antagonistes muscariniques non sélectifs. L’inactivation chimique du muscle ciliaire s’accompagne d’un blocage de l’iridoconstriction et donc d’une mydriase plus ou moins importante selon les sujets et les molécules utilisées.
Il existe une autre possibilité de bloquer l’accommodation par stimulation du système orthosympathique dont le médiateur est cette fois l’adrénaline. L’instillation locale du sympathicomimétique représenté par la phényléphrine (Néosynéphrine®) a un effet principalement dilatateur et modérément antiaccommodatif.
Répondant à cette définition nous avons à notre disposition quatre molécules : l’atropine, le cyclopentolate, l’homatropine, le tropicamide.
L’atropine est un alcaloïde naturel extrait de la belladone, famille des Solanacées. Elle est commercialisée sous forme de sulfate d’atropine aux dosages de 0,30 %, 0,50 % et 1 %.
Bien qu’il n’existe aucune donnée précise, il est généralement admis que l’efficacité augmente avec la durée d’instillation [6, 21]. Toutefois, la saturation des sites muscariniques ne semble pas progresser de façon arithmétique. Le protocole habituellement conseillé est d’une goutte matin et soir pendant les cinq jours qui précèdent la consultation et une goutte le matin de la consultation. Avant l’âge de deux ans, il faut utiliser le dosage à 0,30 % ; 0,5 % de deux à cinq ans ; 1 % au-dessus de cinq ans.
La molécule d’atropine est loin d’être anodine car sa diffusion accidentelle atteint d’autres sites de l’organisme. Le risque majeur de tout surdosage est le déclenchement d’une tachycardie qui peut être fatale. Cette circonstance est heureusement exceptionnelle et résulte toujours d’un non-respect de précautions élémentaires avec, à l’extrême, une ingestion par jeu du contenu du flacon (10 ml = dose létale).
Il est donc nécessaire de prévenir les parents des précautions à prendre : ne pas dépasser les instillations prévues, obturer autant que possible les points lacrymaux et surtout ne jamais laisser les flacons à portée de tout enfant. Il sera conseillé de rapporter les flacons en pharmacie ou au cabinet.
De façon relativement fréquente, on rencontre des incidents bénins : rougeur ou œdème du visage, poussée de fièvre, agitation, troubles digestifs. Ceux-ci cessent généralement de façon rapide à l’arrêt des instillations. Des eczémas peuvent également survenir lors d’une utilisation prolongée dans le traitement de l’amblyopie.
Dans la pratique, l’inconvénient majeur est l’effet rémanent de cinq à dix jours qui rend difficile l’utilisation répétée au-delà de deux à trois ans et en période estivale.
Le cyclopentolate est un composé de synthèse qui est commercialisé en France sous forme de chlorhydrate de cyclopentolate au dosage de 0,5 %.
À la différence de l’atropine sa mise en action optimale est rapide et son effet de rémanence est court, de dix à vingt-quatre heures.
Le protocole de référence correspondant aux premières validations AMM est l’utilisation d’une goutte aux temps T0, T5 et T10 avec examen réfractif réalisé entre T45 et T60 [38, 44]. Des études ont montré qu’un résultat identique pouvait être obtenu avec seulement deux instillations [20]. Cependant, en dehors des conditions idéales des expérimentations, on observe souvent des instillations rendues plus ou moins inefficaces par occlusion trop rapide des paupières et il reste préférable de respecter le protocole de base.
Le risque principal est le déclenchement d’une crise épileptique lorsque le contexte est méconnu ou le traitement non suivi. Cette complication est d’ailleurs surtout le fait du dosage à 1 % commercialisé uniquement à l’étranger ; aucun accident mortel n’a été signalé.
La précaution élémentaire est donc de poser systématiquement la question des antécédents de toute pathologie neurologique.
Parmi les incidents bénins il est en revanche assez fréquent de constater des états de somnolence.
Indépendamment de ces incidents, il faut rappeler que le cyclopentolate n’a pas l’AMM au-dessous de l’âge d’un an, mais uniquement parce que les phases habituelles d’essais n’ont été ni demandées ni réalisées. En pratique, ceci n’est pas un obstacle réel pour son utilisation avant un an.
L’homatropine est un dérivé de synthèse de l’atropine commercialisé sous forme de bromhydrate d’homatropine dans un dosage à 1 %.
Il n’existe pas de protocole connu ou conseillé pour les examens réfractifs. Dans les études comparatives menées par Péchereau [36], un protocole identique à celui du cyclopentolate a été adopté avec instillations à T0, T5 et T10. La réfraction maximale a été notée à T60.
Il n’y a aucune mention sur ce sujet dans la littérature.
Le tropicamide agit selon le même principe que l’atropine. Il est commercialisé dans un dosage à 0,50 %.
Le protocole conseillé dans le Vidal est de quatre à six instillations à cinq minutes d’intervalle avec examen réfractif trente minutes après la dernière instillation. Dans les études comparatives avec instillations à T0, T5 et T10, Péchereau a trouvé un effet maximal entre T30 et T45 [36].
En théorie, les effets secondaires sont ceux rencontrés avec l’atropine mais, avec les protocoles habituels, il n’y a en principe aucun risque particulier. La rémanence d’effet est de quatre à cinq heures.
Bien qu’il n’existe apparemment aucun protocole parfait, on constate globalement un consensus sur une hiérarchie, laquelle est parfaitement illustrée dans les différentes études comparatives précédemment citées [36]. Dans la grande majorité des observations, l’atropine a un effet supérieur à celui du cyclopentolate de l’ordre de 0,30 à 0,50 d ; ce dernier a lui-même un effet supérieur à celui de l’homatropine et du tropicamide pour les mêmes valeurs.
Cependant, il faut nuancer cette hiérarchie qui peut présenter des écarts nettement supérieurs en fonction des individus (iris clairs versus iris foncés), selon l’amétropie (spasmes accommodatifs des forts hypermétropes), et selon le contexte (premier bilan ou correction optique portée). Ainsi, la variabilité d’efficacité entre les différentes molécules est certainement maximale lorsqu’il s’agit d’un examen de première intention et dans un contexte de pathologie sensorimotrice. Ces différences ont tendance à s’amenuiser dès lors qu’il existe une correction optique adaptée, plus particulièrement une correction optique totale dont le port est permanent. Dans certaines conditions, quand le traitement a été suffisamment long pour libérer la totalité de l’hypermétropie latente, il n’y a le plus souvent aucune différence entre l’effet de l’atropine et celui du cyclopentolate.
Ces constats reviennent à dire que le meilleur cycloplégique n’est pas d’ordre pharmacologique mais est bien représenté par le port permanent de la correction optique totale qui seule permet de libérer à terme les spasmes accommodatifs les plus rebelles.
Les examens cycloplégiques itératifs sont néanmoins nécessaires pour la mise à jour régulière de la réfraction optimale.
L’efficacité des cycloplégiques n’étant souvent pas totale lors des premiers examens, il peut être intéressant de rechercher une potentialisation en associant plusieurs molécules dès lors qu’on ne veut plus utiliser l’atropine [9, 27]. Il n’existe pas de forme commercialisée de ces associations.
L’association la plus classique est celle du cyclopentolate et du tropicamide, dont l’efficacité a été confirmée.
Une association également retrouvée dans la littérature est celle du cyclopentolate et de la phényléphrine. On rappellera que cette dernière molécule est principalement un dilatateur mais sa potentialisation est confirmée par certains auteurs. Il faut surtout insister sur le fait que cette molécule est connue de longue date pour des risques cardiovasculaires et est donc à éviter chez le jeune enfant. Cet effet a récemment été confirmé pour le dosage à 10 % en dessous de douze ans et pour le dosage à 5 % pour le nouveau-né (information Europhta 2011).
À titre personnel, nous avons utilisé chez le nouveau-né une association homatropine-tropicamide à raison d’une goutte à T0 avec skiascopie entre T30 et T45. Bien que cette association laisse attendre une sous-estimation de la réfraction, les contrôles réalisés entre un mois et quatre mois plus tard sous atropine ont montré une estimation très satisfaisante. En effet, la variation réfractive moyenne pour plus de trois cents enfants a été quasi nulle, mais avec des variations individuelles notables. En dehors de situations d’emblée pathologiques, un tel protocole avec plusieurs instillations a l’avantage d’être dénué de tout risque apparent dans ce jeune âge.
Les résultats exposés précédemment confirment que, sur le plan de l’efficacité et de la fiabilité, il n’existe que deux vrais cycloplégiques : l’atropine et le cyclopentolate.
L’atropine est le cycloplégique de référence parce que le plus efficace dans son protocole minimal de cinq à six jours, permettant ainsi d’atteindre d’emblée le meilleur point de départ possible pour une éventuelle correction optique.
L’atropine est donc a priori d’indication idéale pour le premier examen, en particulier lorsqu’il est motivé par une pathologie sensorimotrice suspectée ou avérée.
Compte tenu de leur rareté, les complications graves ne sont nullement un obstacle à cette démarche.
Le cyclopentolate peut être défini comme le cycloplégique de base. En effet à partir de l’âge de deux à trois ans, l’utilisation itérative de l’atropine devient nettement gênante et le relais est nécessairement pris par le cyclopentolate. C’est également l’indication de choix de tout examen réalisé pendant la scolarité et chez l’adulte en première intention.
Le choix du cyclopentolate peut également se justifier chez le tout jeune enfant en première consultation. En effet, lorsque le domicile des consultants est éloigné, circonstance fréquente dans la pathologie oculomotrice, un examen sous cyclopentolate permet une prescription immédiate. C’est seulement lors du second contrôle que le protocole d’atropine permettra de vérifier les résultats du premier examen.
Au total, le choix entre ces deux cycloplégiques, reste lié aux circonstances d’examen, l’essentiel étant de réaliser chaque fois que la clinique l’impose au minimum un bilan avec le cycloplégique de référence. Cela est évident pour le jeune enfant dont on connaît la puissance accommodative. Mais cette indication peut concerner l’adulte en cas de spasme accommodatif rebelle, surtout avant une éventuelle décision chirurgicale.
L’utilisation d’un cycloplégique mineur, plus particulièrement du tropicamide, peut s’avérer utile dans un contexte d’insuffisance motrice cérébrale ou autre pathologie neurologique. Ce choix n’est en revanche pas justifié pour des examens de dépistage réfractif systématique pratiqués avant un an.
Quel que soit le cycloplégique utilisé ou la méthode de mesure, il persiste une incertitude sur l’accommodation résiduelle. La mesure subjective de l’acuité en vision de loin représente l’examen le plus fiable, qualifié de « juge de paix ». Elle nécessite un minimum de coopération et correspond par conséquent à l’âge d’utilisation du cyclopentolate. Des études prospectives nous ont montré que si dans 80 % des cas il existait une excellente correspondance (0 ± 0,25 d), dans les 20 % restants on constate des écarts plus ou moins manifestes liés très probablement à une rigueur insuffisante des instillations.
Nous avons à notre disposition deux cycloplégiques majeurs, l’atropine et le cyclopentolate, dont l’utilisation est la base incontournable de tout bilan réfractif. Ce n’est qu’en cas de contre-indication de ces deux molécules qu’on peut faire appel à un cycloplégique mineur, habituellement le tropicamide. Une potentialisation du cyclopentolate par le tropicamide peut être ponctuellement utile. C’est cependant la seule correction optique totale en port permanent qui permet d’obtenir le contrôle total de l’accommodation.
La plupart des travaux concernant la réfraction analysent l’évolution de manière globale, exprimant une moyenne et une dispersion en termes d’écart-type. Le jeune enfant serait ainsi moyennement hypermétrope de l’ordre de 2 d avec une distribution de type gaussien. À partir de l’adolescence, on observerait une nette concentration des réfractions autour d’une faible hypermétropie avec une courbe nettement pointue. Une telle description ne donne qu’une vision particulière de la question et n’apporte en fait que peu d’éléments pratiques quant au cursus réel des réfractions individuelles. Elle a surtout le désavantage de mélanger des situations réfractives totalement différentes dans leurs potentialités évolutives.
C’est donc à une analyse de type différentiel en fonction des divers degrés réfractifs qu’il faut accorder une préférence. Cette approche permet ainsi de définir les limites de la réfraction physiologique au-delà desquelles se trouve le domaine des amétropies. Parmi ces amétropies, on distinguera les situations d’orthophorie et celles de strabisme.
La description globale permet de mettre en évidence un élément caractéristique de l’adaptation anatomique aux besoins d’un fonctionnement visuel optimal. Il s’agit du phénomène d’emmétropisation qui a pour but de corriger les anomalies réfractives éventuelles présentes à la naissance. Il s’agit donc ici d’une définition fonctionnelle. Ce mécanisme est retrouvé dans une partie importante du monde animal. Ces correctifs portent sur les trois paramètres réfractifs : sphère, cylindre et anisométropie.
Il faut insister d’emblée sur la difficulté à établir une courbe d’évolution. En effet les études transversales proposées dans la littérature sont parcellaires et sont le plus souvent obtenues sans cycloplégie. Les études longitudinales pour leur part exposent rapidement à des pertes progressives importantes par rapport à l’échantillon initial, ce qui conduit à des biais notables de sélection et d’analyse. Par ailleurs, l’inclusion ou non de sujets strabiques induit des variations significatives dans les différents paramètres. Les courbes présentées ici sont donc par nécessité une combinaison de plusieurs études longitudinales débutant à des âges différents et après exclusion des strabismes.
La situation réfractive du nouveau-né a donné lieu à de nombreux travaux avec des résultats plus ou moins discordants. Actuellement, il existe plutôt un certain consensus autour d’une hypermétropie nette de l’ordre d’au moins 3 d. La dispersion autour de cette moyenne est plutôt modérée, de l’ordre de 1,50 d.
C’est la période la moins étudiée bien qu’elle soit pourtant essentielle pour l’avenir réfractif. On observe en effet une régression nette et rapide de l’hypermétropie néonatale qui est en moyenne diminuée de moitié dans une régression quasi arithmétique, conduisant entre le neuvième mois et le douzième mois à une valeur moyenne de + 1,50 d à + 1,75 d (en équivalent sphérique, ES). Cette emmétropisation qu’on peut qualifier de précoce est de loin la plus importante sur le plan fonctionnel (fig. 4-4a).
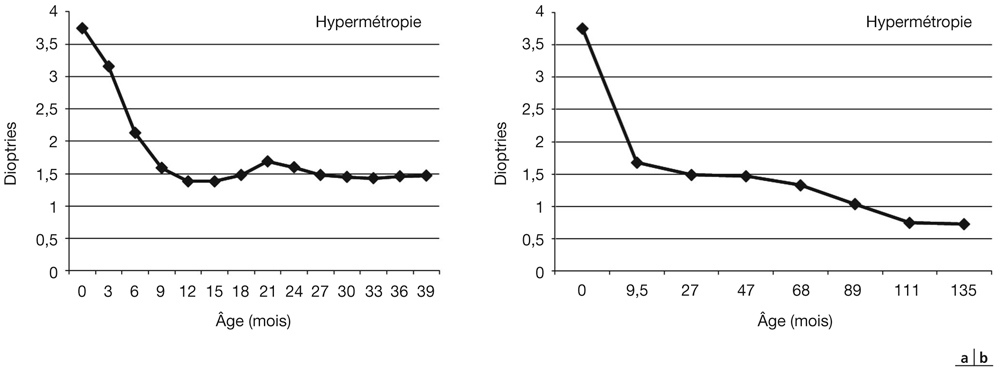
Fig. 4-4 Dans une population non strabique, évolution (étude longitudinale) de l’hypermétropie.
a. De la naissance à 3 ans (39 mois). b. De la naissance à 11 ans (135 mois).
On observe une lente régression de l’hypermétropie qui conduit à une situation dite d’emmétropie fonctionnelle, correspondant à une réfraction de + 0,50 d à + 0,75 d. On peut définir cette période comme celle de l’emmétropisation tardive (fig. 4-4b). Progressivement, la distribution autour de cette moyenne perd son caractère gaussien, la courbe devenant de plus en plus pointue (leptokurtique). Cette description correspond à la définition statistique de l’emmétropisation. Pour des raisons de biais de sélection précédemment expliqués, nos études s’arrêtent actuellement à l’âge de onze à douze ans.
Un certain nombre de travaux expriment une nette tendance à la myopie qui se traduit par une augmentation de son épidémiologie. Ultérieurement apparaît un retour vers l’emmétropisation. Cette interprétation de l’évolution réfractive est probablement erronée. Il est en effet difficile d’imaginer que les modifications anatomiques éventuellement liées à l’âge transforment les myopes en hypermétropes. D’ailleurs, si les surcorrections myopiques sont classiques, elles sont en règle très modérées et n’ont pas d’impact significatif. Cette évolution paradoxale est en fait principalement liée à un biais de sélection. Entre vingt et cinquante ans, les sujets emmétropes ou faiblement hypermétropes ne consultent pas, à l’inverse des myopes, et un nouvel équilibre épidémiologique se rétablit sous l’effet de la presbytie. À la différence des myopes, les hypermétropes libèrent souvent leur composante latente qui peut atteindre plusieurs dioptries. Cette évolution réfractive typique chez les Caucasiens devient pratiquement absente pour les populations de l’est asiatique chez qui on sait qu’en une génération la prévalence myopique a doublé aussi bien chez les enfants que chez les adultes. Un certain nombre d’indices montrent que cette mutation a commencé à montrer ses effets en Europe.
Contrairement à celle de la sphère, la valeur moyenne de l’astigmatisme absolu est très modérée. Mais la caractéristique principale, confirmée dans plusieurs publications, est que la valeur maximale n’est pas observée à la naissance mais entre le quatrième et le cinquième mois (fig. 4-5a). Ce maximum reste inférieur à 1 d et se stabilise ensuite dans une valeur inférieure à 0,50 d (fig. 4-5b).
Au cours de la première année, les astigmatismes réels sont directs en large majorité. Ils sont plutôt inverses d’un an à quatre ans.
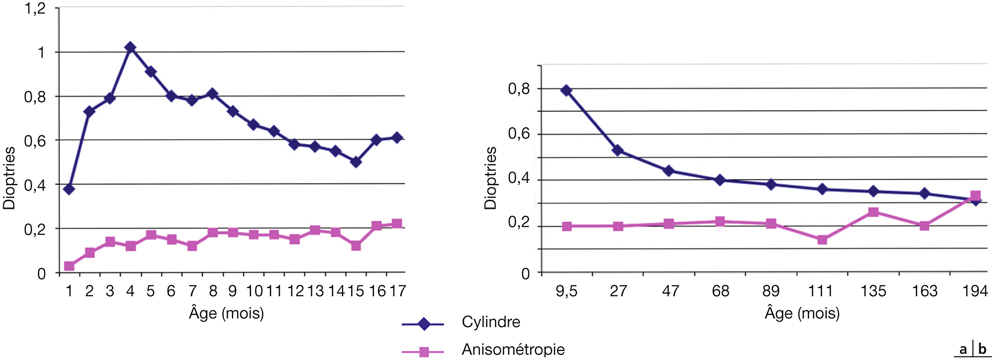
Fig. 4-5 Dans une population non strabique, évolution (étude longitudinale) du cylindre et de l’anisométropie.
a. De la naissance à 1 an (17 mois). b. De 9 mois à 16 ans (194 mois).
Une des caractéristiques de la réfraction humaine est qu’en termes de statistique, l’œil gauche est le miroir de l’œil droit. Cela se traduit par le constat que l’anisométropie moyenne sphérique ou cylindrique est faible en valeur, inférieure à 0,25 d (fig. 4-5), et en prévalence, inférieure à 5 %. Il est également classique de constater que la majorité des anisométropies présentes avant l’âge d’un an vont disparaître, alors que celles constatées plus tard sont généralement secondaires et souvent le témoin d’un processus amblyopique.
L’évolution de la moyenne réfractive est en principe l’expression d’une adaptation anatomique pour un fonctionnement visuel optimal. Cette évolution correspond au phénomène d’emmétropisation qui comporte en réalité deux phases successives :
-
la première est clairement observée au cours de la première année : il s’agit d’un processus rapide et important qui est censé placer d’emblée l’œil dans une situation fonctionnelle très favorable ;
-
la seconde, beaucoup plus lente et prolongée, est censée amener l’optique oculaire dans l’étroite marge physiologique.
La réfraction physiologique peut se définir comme l’ensemble des réfractions qui, à un âge donné, permettent une acuité normale en l’absence prolongée de tout signe fonctionnel.
Pendant la période où on ne dispose pas de contrôle subjectif, c’est-à-dire jusqu’à environ trois ans, les valeurs de référence reposent sur la notion de facteurs de risque d’amblyopie et de strabisme ainsi que sur les implications visuelles théoriques des anomalies optiques. Au-delà des trois ans, la confrontation des données objectives et subjectives donne des indications suffisamment claires.
La limite supérieure a été définie par la notion de facteur de risque et se situe approximativement à 4 d d’hypermétropie à six mois (en équivalent sphérique). Celle-ci s’abaisse progressivement de façon régulière pour atteindre une valeur d’environ 1,25 d à l’adolescence, avec comme point de repère à l’âge de dix ans une hypermétropie critique de 1,75 d à 2,00 d (fig. 4-6).
La limite inférieure devrait en théorie être le zéro réfractif. En réalité, on sait que le fonctionnement visuel optimal n’est pas atteint avant l’âge de quatre à cinq ans et que logiquement une faible amétropie n’est normalement pas identifiée par les structures rétinocorticales. En conséquence, une myopie modérée reste tolérable. En appliquant les lois de l’optique, cette myopie devra être inférieure à 2 d à six mois pour diminuer rapidement et avoir disparu entre quatre ans et cinq ans.
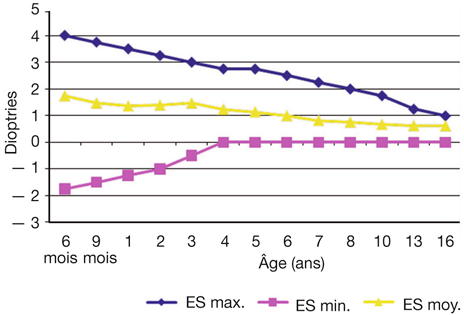
Fig. 4-6 Dans une population non strabique, évolution (étude longitudinale) de l’équivalent sphérique de 6 mois à 16 ans (moyenne, limite physiologique basse et haute).
L’évolution des limites pour l’astigmatisme suit le même principe mais avec deux caractéristiques : d’une part il existe une quasi-symétrie entre astigmatismes directs et inverses ; surtout, la régression vers des valeurs faibles est beaucoup plus rapide puisque cet astigmatisme ne doit plus dépasser 0,50 d à partir de quatre ou cinq ans. Statistiquement, il n’y a plus d’astigmatisme à partir de dix ans (fig. 4-7).
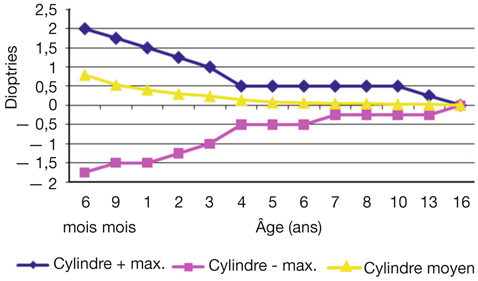
Fig. 4-7 Dans une population non strabique, évolution (étude longitudinale) de l’astigmatisme (cylindre) de 6 mois à 16 ans (moyenne, limite physiologique basse et haute).
Comme pour l’astigmatisme, une valeur de 0,50 d ne doit plus être dépassée à partir de quatre à cinq ans. Mais avant l’âge d’un an, toute anisométropie dépassant 1 d est suspecte, surtout si elle persiste à deux examens consécutifs. Les limites sont identiques pour la sphère et le cylindre (fig. 4-8).
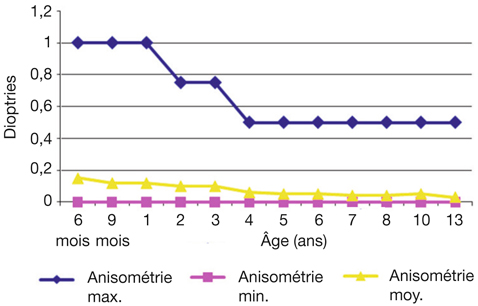
Fig. 4-8 Dans une population non strabique, évolution (étude longitudinale) de l’anisométropie sphérique de 6 mois à 16 ans (moyenne, limite physiologique basse et haute).
Le seul moyen véritable de comprendre le devenir des amétropies est donc d’en réaliser une analyse différentielle en fonction du degré initial de la réfraction. Seules les études longitudinales apportent des renseignements pertinents sur l’historique évolutif de chaque groupe. La difficulté essentielle de ces études est la perte progressive des sujets à chaque nouveau contrôle, avec le risque évident de sélectionner les observations les plus défavorables. Il est donc essentiel d’avoir des études prospectives de grande ampleur.
En dépit de la quasi-absence d’études répondant de façon satisfaisante aux exigences requises, il existe un certain consensus sur le devenir de la plupart des groupes réfractifs.
En ce qui concerne l’étude prospective (à partir de neuf mois), ces constats sont les suivants (fig. 4-9a) :
-
les différents groupes réfractifs ont un trajet approximativement parallèle (donc une absence de convergence d’ensemble vers une réfraction cible) ;
-
l’examen du neuvième mois montre pour la majorité des cas (à l’exception des myopies) le degré le plus élevé des réfractions ;
-
en dehors de quelques nuances, on constate une certaine stabilité jusqu’à l’âge de cinq ans ; la seule exception est notée pour les myopies qui ont plutôt tendance à régresser ;
-
à partir de cinq ans, l’hypermétropie a une évolution régressive avec deux exceptions : les hypermétropies supérieures à 6 d n’ont statistiquement aucune tendance à diminuer et le contingent myopique a pour sa part une nette tendance à s’aggraver, y compris le groupe qui semblait évoluer vers l’emmétropie ;
-
mais le fait le plus important est qu’en dépit de l’amélioration générale des réfractions, on constate sans ambiguïté que de manière globale les hypermétropies supérieures à + 3,75 d lors de l’examen sous cycloplégie au neuvième mois se retrouvent pour la plupart au-dessus de la limite physiologique de + 2,00 d à l’âge de dix ans ;
-
quant au contingent des réfractions initialement physiologiques, on distingue deux sous-groupes :
-
le premier concerne les réfractions supérieures à + 1,25 d et dont l’évolution se fait généralement vers l’emmétropie fonctionnelle ;
-
le second avec des réfractions comprises entre 0 et + 1,25 d présente une tendance nettement moins favorable puisque sa moyenne statistique passe en myopie ; d’ailleurs, la totalité des études rétrospectives réalisées chez les myopes montrent que le point de départ le plus fréquent se situe effectivement dans la faible hypermétropie.
-
Lorsque les données sont analysées de manière rétrospective, le point de référence se situant à la sixième année, on constate que pour nombre de réfractions la valeur la plus élevée n’est pas constatée au neuvième mois mais qu’il existe une hypermétropie latente libérée seulement sous l’effet des corrections optiques (fig. 4-9b). Ce constat met parfaitement en évidence le fait que l’emmétropisation est loin d’être le schéma général.
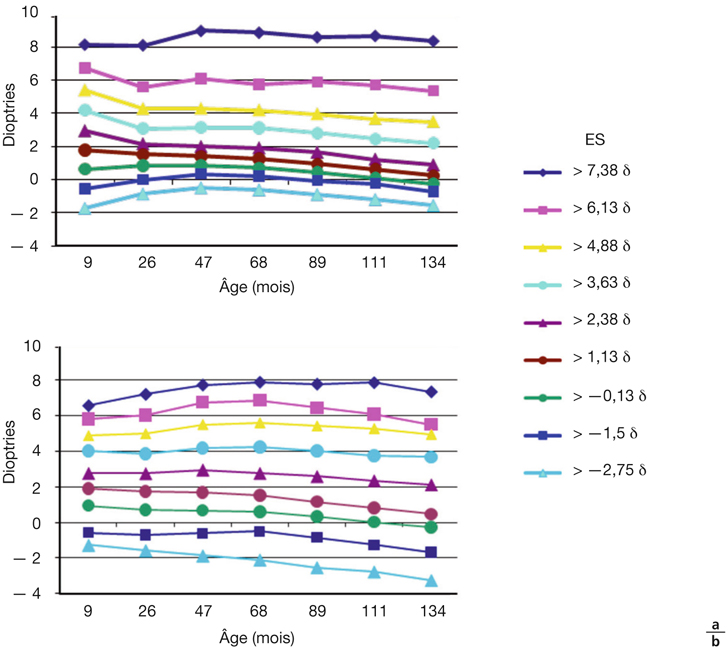
Fig. 4-9 Dans une population non strabique, évolution (étude longitudinale) de la sphère de 9 mois à 11 ans (134 mois) par groupe réfractif.
a. En fonction de la réfraction initiale. b. En fonction de la réfraction à 6 ans.
Dans l’analyse prospective, on observe une régression nette des astigmatismes avec l’âge. Cette régression est d’autant plus marquée que l’astigmatisme initial était important. Néanmoins, on constate comme pour la sphère que le groupe des astigmatismes non physiologiques termine sa course en dehors des limites physiologiques (fig. 4-10a). Comme précédemment, l’analyse rétrospective montre sans ambiguïté l’évolution plus défavorable des forts astigmatismes (fig. 4-10b).
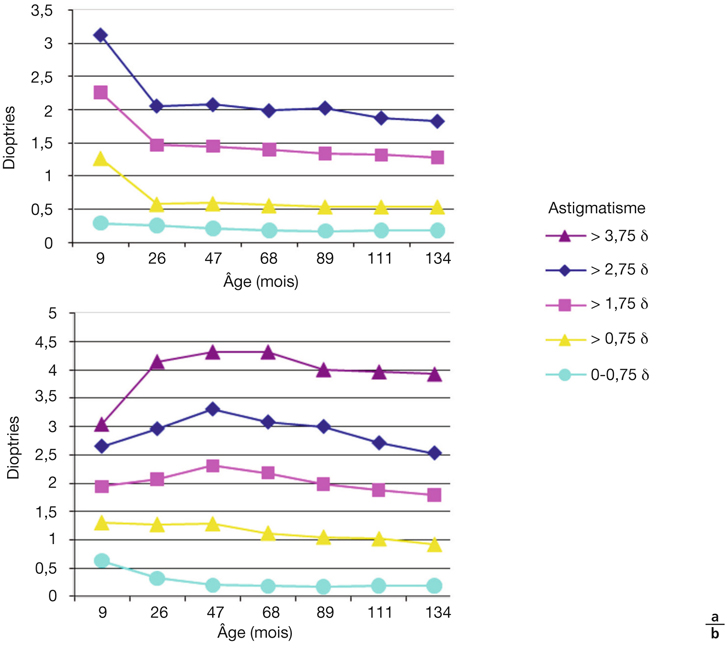
Fig. 4-10 Dans une population non strabique, évolution (étude longitudinale) de l’astigmatisme de 9 mois à 11 ans (134 mois) par groupe réfractif.
a. En fonction de la réfraction initiale. b. En fonction de la réfraction à 6 ans.
Le comportement des anisométropies est calqué sur celui des paramètres précédents avec une tendance nette pour les fortes anisométropies à persister dans des valeurs significatives (fig. 4-11a).
L’analyse rétrospective illustre parfaitement la notion d’apparition secondaire de l’anisométropie (fig. 4-11b).
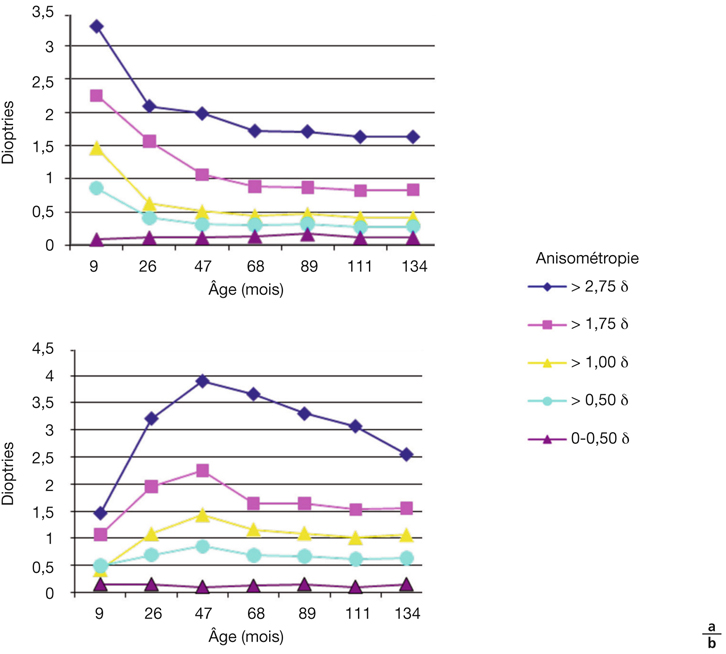
Fig. 4-11 Dans une population non strabique, évolution (étude longitudinale) de l’anisométropie de 9 mois à 11 ans (134 mois) par groupe réfractif.
a. En fonction de la réfraction initiale. b. En fonction de la réfraction à 6 ans.
Une classification des amétropies en trois degrés (« très fortes », « fortes », « moyennes ») permet de constater sur un échantillon d’examens systématiques (sans contexte pathologique) respectivement une prévalence de 2,3 %, 3,8 % et 13,8 % d’amétropies significatives, soit un total de 20 % de la population (tableau 4-I). Devant ces chiffres on peut confirmer que le processus initial d’emmétropisation est loin d’être la règle.
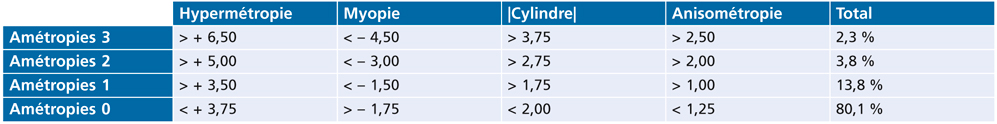
Tableau 4-I – Classification des amétropies en quatre degrés à l’âge de 9 mois dans le cadre d’un examen systématique. Très fortes : 3. Fortes : 2. Moyennes : 1. Absence d’amétropie : 0.
L’analyse longitudinale différentielle présentée précédemment décrit le comportement moyen des différents groupes réfractifs. Cependant, à l’intérieur de chacun de ces groupes, l’évolution n’est pas identique pour tous les individus. Une certaine proportion d’entre eux va avoir une évolution favorable. Ce constat permet de chiffrer ce que l’on peut qualifier de « taux d’emmétropisation ». Ainsi, dans le groupe des très fortes amétropies et en fonction des différents paramètres, ce taux va de 5 % à 25 %. Pour les fortes amétropies, il est de 20 % à 45 %. Pour les amétropies moyennes, il atteint 50 % à 80 %. Enfin, le groupe initialement physiologique n’est pas confirmé à 100 % puisque 10 % à 20 % des observations passent dans la classe des amétropies, principalement en raison du resserrement des limites physiologiques.
Sur un plan pratique, le suivi longitudinal de l’échantillon précédent jusqu’à l’âge de sept ans (80 % de contrôles effectifs) a montré une confirmation amétropique pour les trois degrés réfractifs de 96,6 %, 85,4 % et 57,9 % respectivement. Le groupe physiologique a, pour sa part, montré une évolution défavorable de 11,4 % à 19,3 % selon que les réfractions étaient situées au-dessous ou au-dessus de la moyenne réfractive du groupe. La survenue de strabismes apparaît pour sa part plus particulièrement liée aux fortes amétropies. Le résultat global de l’évolution est ainsi de 28 %, confirmant que les échecs précoces de l’emmétropisation ne seront pour la plupart pas rattrapés (tableau 4-II).
Cela devrait logiquement être un argument majeur pour l’intérêt d’un dépistage cycloplégique précoce des amétropies.
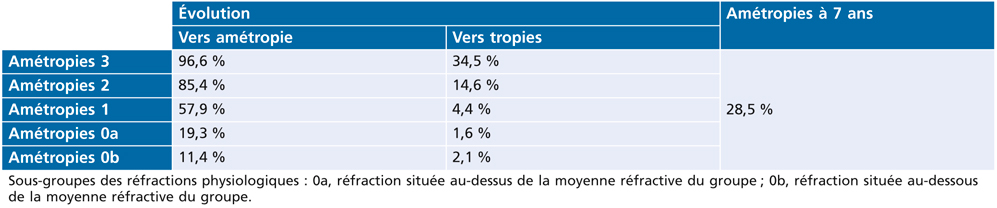
Tableau 4-II – Suivi longitudinal de l’échantillon précédent jusqu’à l’âge de 7 ans (80 % de contrôles effectifs).
La population strabique présente un certain nombre de particularités :
-
pour des raisons diverses, les premiers bilans réfractifs ne sont souvent pas obtenus avant l’âge de vingt-quatre à trente mois ;
-
la décompensation de l’hypermétropie latente qu’on retrouve dans une partie de la population orthophorique devient pratiquement la règle chez le strabique ; le maximum réfractif est en moyenne constaté vers l’âge de six ans.
Au moins pour ces deux raisons, l’analyse à partir de cette référence maximale paraît la plus adaptée d’autant qu’elle permet un taux de suivi largement supérieur à 50 % entre deux et dix-sept ans.
Si les ésotropies et les exotropies présentent un schéma évolutif similaire, la différence nette entre leur réfraction moyenne justifie une étude séparée (fig. 4-12).
On sait que dès l’identification du strabisme, 40 % à 50 % des observations présentent une réfraction sphérique au moins égale à + 3,50 d. Cette situation n’exclut pas la réalité de réfractions plus faibles, y compris myopiques. Comme pour les sujets orthophoriques, l’addition de ces deux populations aboutit à une moyenne sans signification réelle et qui n’a donc aucune valeur indicatrice sur le plan évolutif.
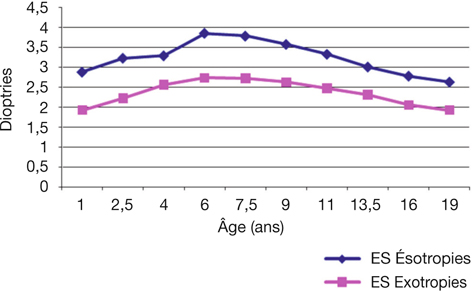
Fig. 4-12 Dans une population strabique, évolution (étude longitudinale) de la sphère de 1 an à 19 ans en fonction du type de déviation (ésotropie ou exotropie initiales).
L’évolution cylindrique ne présente aucune particularité, avec une stabilité dans le temps (fig. 4-13). Inversement, l’anisométropie présente une tendance à l’accentuation progressive (fig. 4-14).
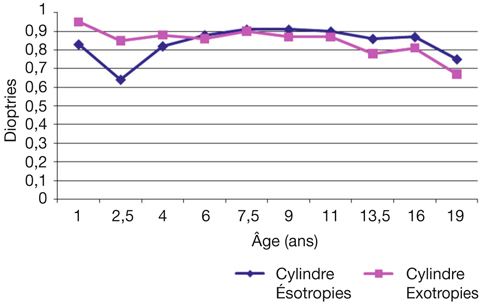
Fig. 4-13 Dans une population strabique, évolution (étude longitudinale) de l’astigmatisme de 1 an à 19 ans en fonction du type de déviation (ésotropie ou exotropie initiales).
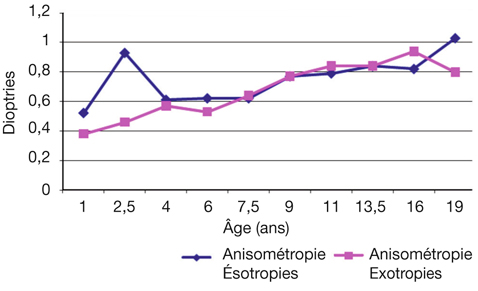
Fig. 4-14 Dans une population strabique, évolution (étude longitudinale) de l’anisométropie de 1 an à 19 ans en fonction du type de déviation (ésotropie ou exotropie initiales).
Comme en cas d’orthophorie, l’analyse différentielle permet de distinguer clairement plusieurs modalités évolutives (fig. 4-15) :
-
pour l’ensemble des groupes comportant une hypermétropie initiale supérieure à + 2,00 d, on constate une décompensation significative de l’hypermétropie latente ; surtout, l’hypermétropie finale apparaît identique à celle détectée lors de la découverte du strabisme ;
-
à l’opposé, le groupe des myopes a un comportement strictement identique à celui observé en l’absence de strabisme : on note une régression initiale modérée de la myopie qui est considérée comme un signe d’emmétropisation ; mais, à partir de sept à huit ans, la myopie reprend le plus souvent une évolution avec ses variations classiques ;
-
le groupe des réfractions physiologiques présente, comme pour les sujets orthophoriques, soit une tendance à une hypermétropie modérée mais nécessitant une correction compte tenu du strabisme, soit une évolution vers la myopie.
Le constat important est que les ésotropies et les exotropies ont le même modèle évolutif pour des tranches réfractives identiques, la moyenne exotropique étant seulement un peu plus faible.
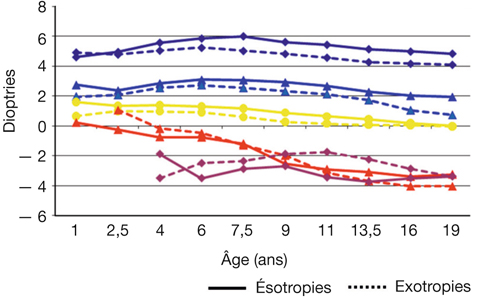
Fig. 4-15 Dans une population strabique, évolution (étude longitudinale) de la sphère de 1 an à 19 ans en fonction du type de déviation (ésotropie ou exotropie initiales) et de la réfraction initiale.
Comme chez l’orthophorique les astigmatismes non physiologiques ont tendance à persister, tandis que les astigmatismes physiologiques conservent plutôt cet état (fig. 4-16). À l’inverse, il n’est observé aucune régression sur le long terme même pour les anisométropies modérées (fig. 4-17).
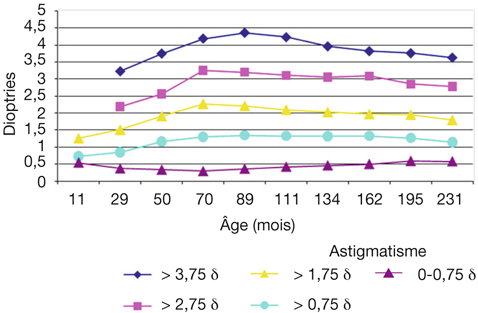
Fig. 4-16 Dans une population strabique, évolution (étude longitudinale) de l’astigmatisme de 1 an (11 mois) à 19 ans (231 mois) par groupe réfractif en fonction de la réfraction initiale.
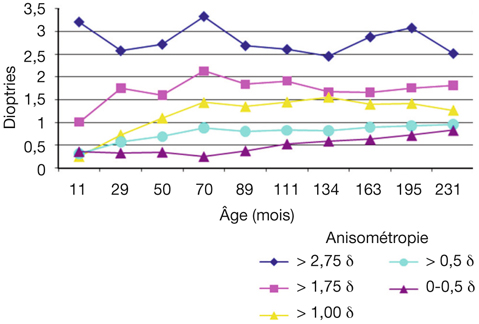
Fig. 4-17 Dans une population strabique, évolution (étude longitudinale) de l’anisométropie de 1 an (11 mois) à 19 ans (231 mois) par groupe réfractif en fonction de la réfraction initiale.
Une étude identique à celle menée chez les sujets orthophoriques entre quarante et soixante ans a montré l’existence fréquente d’une sous-correction, modérée en moyenne (1,00 d) mais avec 20 % des cas supérieurs à 2,00 d, les réfractions hypermétropiques étant les plus exposées. La réfraction des strabismes semble stabilisée entre vingt ans et vingt-cinq ans. Les ésotropies restent globalement nettement hypermétropes avec un nombre modéré de myopies de l’ordre de 15 %. Les exotropies sont caractérisées par un taux de myopie nettement plus élevé, probablement 30 % à 35 %, mais avec un pourcentage au moins identique d’hypermétropies significatives.
Toutes les analyses confirment que l’adulte strabique est généralement sous-corrigé pendant une longue période de sa vie et que les valeurs notées sous cycloplégie à l’adolescence seront retrouvées au bout de la presbytie ou lors d’un bilan pour chirurgie tardive.
L’étude de l’évolution globale exprime principalement le phénomène d’emmétropisation mais masque totalement la diversité des situations individuelles. La connaissance précise des limites de la réfraction physiologique en fonction de l’âge permet de prendre les mesures préventives et curatives optimales pour l’avenir visuel et moteur du jeune enfant. Seule l’analyse différentielle rend compte des tendances évolutives des différents degrés réfractifs ; le mode prospectif et le mode rétrospectif apportent chacun des renseignements qui semblent contradictoires mais sont en réalité complémentaires : le phénomène d’emmétropisation est loin d’être la règle. Ceci se traduit par une augmentation avec l’âge de l’épidémiologie amétropique. L’analyse de la réfraction strabique est celle qui met le mieux en évidence la notion d’hypermétropie latente. L’identité des ésotropies est indiscutablement marquée par une prévalence élevée et durable des fortes hypermétropies. Celle des exotropies est remarquable par la prévalence élevée des myopies mais aussi des hypermétropies, ce dernier élément les différenciant des orthophories. En revanche, sur le plan évolutif, la réfraction est avant tout liée au degré initial des amétropies et non au statut moteur.
Lorsqu’une correction optique apparaît nécessaire, le choix de sa nature va dépendre de deux ordres de critères :
-
la pathologie présente ou à craindre : strabisme, amblyopie, facteurs de risque, troubles visuels ou fonctionnels ;
-
l’âge d’examen : examen systématique à neuf et vingt-quatre mois, dépistage en PMI entre trois et six ans, suivi scolaire entre sept et dix ans, adultes.
La clinique reste en principe le fil directeur principal.
Le strabisme comportant en tout ou en partie un dérèglement de l’accommodation-convergence, le traitement optique doit être logiquement une correction optique totale. C’est en effet le moyen le plus efficace pour réduire les anomalies du rapport AC/A, en supprimant tous les influx accommodatifs liés à l’absence d’emmétropie stricte pour la fixation de loin. Une telle démarche repose sur plusieurs constats :
-
il n’y a pas de relation entre la quantité d’hypermétropie généralement présente et l’angle observé ;
-
la libération du spasme accommodatif présent dans la grande majorité des strabismes n’est généralement obtenue qu’après plusieurs années de port permanent de cette correction optique totale. Ceci a en particulier un impact majeur dans certains strabismes survenus tôt puisque 10 % des ésotropies s’avèrent être en réalité des exotropies (qualifiées de secondaires) avec leur correction réelle.
En conséquence, l’absence de correction des amétropies apparemment faibles de certaines ésotropies précoces ou la sous-correction volontaire systématique conduisent tôt ou tard à un bilan clinique erroné avec ses éventuelles conséquences chirurgicales.
Des obstacles apparents peuvent sembler contrarier ce choix :
-
une correction apparemment non supportée par l’enfant ? En réalité, seules les sous-corrections peuvent ne pas apporter le confort attendu. Après nouveau contrôle cycloplégique, le niveau de correction sera généralement confirmé ; le problème reste lié au caractère de l’enfant et à l’autorité parentale ;
-
la correction optique peut modifier l’angle de façon apparemment défavorable. C’est plutôt le cas des exotropies dont l’angle peut être augmenté, mais parfois aussi de certaines ésotropies dont on modifie l’état sensoriel (récupération de l’amblyopie). Cette situation est en réalité bénéfique car elle révèle la réalité du contexte moteur. Il est très important de prévenir à l’avance les parents de cette éventualité.
Si la prescription de la correction optique totale est essentielle dans la gestion du trouble oculomoteur, elle est souvent insuffisante à elle seule pour lutter contre les perversions sensorielles propres au strabisme avec, le plus souvent, une dominance monoculaire entraînant une neutralisation de l’œil dévié qui conduit dans au moins 50 % des cas à une amblyopie. Cette pathologie sensorielle peut même survenir chez le jeune enfant en cas de parallélisme apparent. Il est donc nécessaire d’adjoindre d’emblée un traitement protecteur représenté par une dissociation oculaire, occlusion ou pénalisation.
Lorsqu’après plusieurs années de ces traitements optiques, les problèmes moteurs et visuels ont été réglés, vient la phase d’entretien. À partir de sept à huit ans et surtout à l’adolescence, il existe un désir fréquent de vouloir supprimer la correction optique, ce qui se manifeste initialement par un abandon plus ou moins fréquent de cette dernière. L’expérience montre que dans la réalité il existe trois situations.
Elles ne se modifient généralement pas avec le temps. Même si, dans ces âges, l’accommodation est suffisamment puissante pour compenser cette hypermétropie et permettre une acuité normale sans correction, les signes fonctionnels puis visuels viendront tôt ou tard rappeler à la réalité. Un nouveau bilan cycloplégique retrouvera le plus souvent l’amétropie initiale. Il n’y a dans ce cas aucun motif à réduire la correction.
Elles ont une réelle tendance à régresser sensiblement mais elles persistent en partie et il faut alors adapter la correction au fil du temps, en restant toujours dans l’esprit de la correction totale qui donne toujours l’acuité optimale.
Une partie notable d’entre elles ont une tendance significative à évoluer vers la myopie mais dans des proportions variables, comme on l’observe dans la population myopique non strabique. Dans ces conditions, l’acceptation de la correction ne doit plus poser de problème.
En consultation de routine, le renouvellement d’une correction optique chez un sujet strabique se fait le plus souvent sans cycloplégie. Néanmoins, en cas de presbytie anormalement précoce ou devant l’apparition de troubles fonctionnels, une cycloplégie au cyclopentolate est utile. Elle devient strictement obligatoire en cas de modification de l’angle et surtout si une intervention est envisagée. Une étude prospective menée sur une série de quarante-trois patients a montré qu’il existait une sous-correction de 1 d à 2 d dans 35 % des cas et supérieure à 2 d dans 21 % des cas. Ces résultats étaient identiques pour trois cent soixante-dix adultes non strabiques.
Dans tous les cas, seul le bilan cycloplégique sous cyclopentolate, voire sous atropine, permet d’adapter la correction au niveau souhaitable, ce qui est un préalable obligatoire à tout acte chirurgical éventuel.
Qu’elle soit purement réfractive ou associée au strabisme, l’amblyopie comporte toujours une altération de l’accommodation, qui cette fois est en principe monolatérale.
Cette altération peut être mise en évidence par des mesures réfractives réalisées sans cycloplégie (photoréfraction, par exemple). La conséquence est que l’évaluation de la réfraction réelle ne peut être réalisée que sous cycloplégie. Une récupération complète et durable ne peut véritablement être obtenue qu’avec la correction optique totale, en principe sur les deux yeux. Dans le déroulement de ce protocole, on constate le plus souvent la réduction de l’anisométropie généralement présente. La variation réfractive la plus importante porte plutôt sur l’œil directeur par décompensation de l’hypermétropie latente.
Si la correction optique totale s’avère nécessaire, elle est, comme dans le strabisme, le plus souvent insuffisante. La dominance oculaire est souvent forte pour l’œil directeur et il est donc essentiel après récupération visuelle de protéger l’isoacuité de façon prolongée (plusieurs années). Le choix de la méthode reste a priori libre entre occlusions intermittentes ou pénalisations. L’essentiel est d’être efficace pour éviter les rechutes.
Qu’il s’agisse de strabisme ou d’amblyopie, le principe de la correction optique totale semble donc un passage obligé. Cependant, les observations issues des expériences de défocalisation optique chez l’animal font craindre que l’utilisation d’une correction optique totale puisse entraver le processus d’emmétropisation en neutralisant l’accommodation [47]. Plusieurs auteurs ont effectivement constaté que la sous-correction de l’hypermétropie chez l’enfant strabique permettait de réduire le degré final de l’amétropie en comparaison de la correction optique totale [17, 40]. Toutefois la diminution de la correction optique, voire sa suppression à terme, ne représente pas l’objectif essentiel du traitement dans le strabisme accommodatif pur ou partiel ; et, outre une notion de confort, il existe dans ce choix une indiscutable connotation psychologique et sociale. Plusieurs auteurs ont à l’inverse souligné que la sous-correction avait un effet négatif sur l’acuité finale [2] ; d’autre part, cette sous-correction favoriserait la détérioration sensorimotrice dont le traitement nécessite une augmentation de la correction et révèle l’absence réelle de régression de l’hypermétropie initiale [8]. La sous-correction dans le strabisme accommodatif ne semble donc apporter aucun bénéfice évident en termes de réfraction et les tentatives d’abandon de la correction sont le plus souvent un échec [39, 43].
En définitive, le traitement de référence dans la durée reste bien la correction optique totale [32].
Une démarche un peu similaire a été adoptée dans la prise en charge du strabisme précoce. Outre l’espérance de permettre le développement de la vision binoculaire, l’intérêt de la chirurgie précoce était de se passer d’une correction optique. Cette option était d’ailleurs encouragée par la notion que le strabique précoce était faiblement amétrope. Nombre de publications ont fait la démonstration qu’au moins sur le plan réfractif cette option aboutissait souvent à un échec par négligence de la participation accommodative liée à une hypermétropie significative [7, 16, 19, 42, 45].
La prise en charge de l’amblyopie réfractive n’a pas non plus échappé au raisonnement du traitement minimaliste qui a été ces dernières années largement diffusé au travers des études PEDIG [5]. La sous-correction et l’occlusion intermittente sont censées apporter d’excellents résultats. Comme cela a été exposé précédemment, la rechute au moins partielle est en réalité le principal aboutissant en l’absence d’un traitement d’entretien sérieux.
L’interprétation qu’on peut donner sur des travaux nettement contradictoires dans leurs conclusions est que tous les sujets ne répondent pas de façon identique aux nécessités de la correction optique [22, 31]. Pour Ingram [23, 24], le défaut d’emmétropisation constaté chez la plupart des strabiques ne serait pas une conséquence de la correction optique totale mais probablement un défaut inné associé à cette pathologie. Pour Clergeau [12], le problème n’est pas spécifiquement lié au trouble oculomoteur mais est dans un rapport largement prédominant avec la seule importance de l’hypermétropie initiale. Si certains patients évoluent spontanément vers l’emmétropie, d’autres vont au-delà puisqu’ils passent en myopie. La majorité d’entre eux restent néanmoins dans un état d’hypermétropie significative. Il est certain qu’une conclusion pertinente ne peut être apportée que sur des observations à long terme ; la période de la presbytie rend définitivement son verdict par rapport à des observations limitées à quelques années de l’enfance ou de l’adolescence.
Des expérimentations cliniques pour évaluer l’intérêt du dépistage systématique sous cycloplégie entre les âges de six et douze mois ont été menées à partir de 1975 par Ingram [25] et par Atkinson [3] et à partir de 1978 par Clergeau [13]. L’analyse longitudinale de ces données a pu déterminer des valeurs critiques pour les différents paramètres réfractifs à partir desquelles il apparaît un risque significatif de strabisme et ou d’amblyopie (tableaux 4-III et 4-IV). Ces situations, qualifiées de facteurs de risque, sont les suivantes :
-
hypermétropie > + 3,50 d ;
-
astigmatisme > 1,50 d ;
-
anisométropie > 1,00 d ;
-
myopie = – 2,00 d.
Il s’agit là de valeurs obtenues sous cycloplégie entre huit et dix mois. Des équivalents en réfraction non cycloplégique ont été également donnés en photoréfraction et autoréfraction, mais ils constituent plutôt une base d’orientation pour le dépistage.
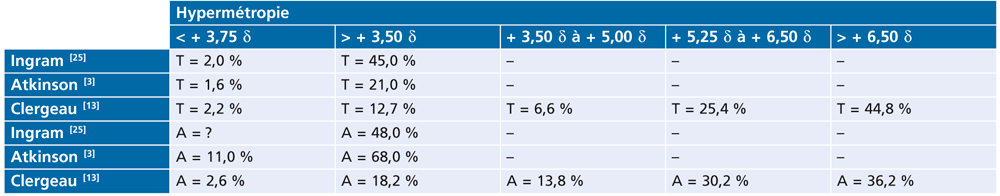
Tableau 4-III – Entre 6 et 12 mois, risque strabique (T) et risque amblyopique (A) en fonction de l’amétropie et selon les auteurs.
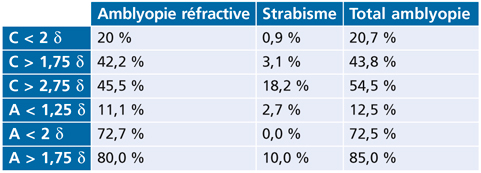
Tableau 4-IV – Risque amblyopique chez des sujets non strabiques en fonction de l’astigmatisme (C) et de l’anisométropie (A).
Le premier axe en termes de prévention est le risque strabique. Ce risque concernant principalement l’hypermétropie apparaît très significatif. La barrière des + 3,50 d (concernant le méridien le plus hypermétrope) amène une augmentation évidente du risque oculomoteur, même si les prévalences sont nettement variables entre les trois auteurs (tableau 4-III). Une analyse sélective en fonction du degré d’hypermétropie permet de mieux mettre en évidence une relation étroite entre le risque et le degré d’hypermétropie. À l’âge de vingt-quatre mois, les valeurs cibles sont quasi identiques.
Le risque étant clairement identifié, il reste à déterminer des règles de prescription. Ces dernières vont être influencées par l’existence ou non d’antécédents familiaux de strabisme.
Il est habituel de considérer le strabisme comme une affection familiale et héréditaire. La réalité est néanmoins un peu plus complexe. En effet, le risque majeur de survenue d’un strabisme chez un enfant examiné à neuf mois est présent principalement lorsque les antécédents strabiques sont du premier degré (parents et fratrie). Le risque est certainement amplifié si les personnes concernées présentent elles-mêmes une hypermétropie significative (+ 3,50 d et plus).
Le second élément qui conforte le risque est la mise en évidence chez l’enfant examiné sous cycloplégie d’une hypermétropie supérieure à + 3,50 d. À partir de cette situation potentielle se dégagent deux orientations.
Le risque étant manifeste, une correction s’impose. L’expérience a montré que pour espérer avoir un rôle préventif, cette correction optique doit être totale. Certes, il n’existe aucune étude prospective ayant exploré rigoureusement cette option. En revanche, tous les protocoles de prévention par correction partielle [4, 26] ont montré leur quasi-inefficacité (peu différente de l’absence de correction), situation confirmée dans nos observations [12].
Si la correction optique totale n’empêche pas la survenue possible d’un strabisme, ce dernier semble le plus souvent être de nature accommodative pure, n’apparaissant qu’à l’ablation des lunettes.
Dans cette situation, il n’y a normalement pas de correction à donner puisque nous sommes dans les limites de la réfraction physiologique. Néanmoins, compte tenu des antécédents, il existe certainement un risque supérieur à celui de la population standard dans la mesure où le strabisme familial sans amétropie significative est une réalité. Dans certains cas, les parents pourront donc préférer opter pour l’essai d’une correction, sachant que là encore il s’agira de la correction totale dont la tolérance n’est pas obligatoirement assurée.
Appliquée à la prévention du strabisme, la correction optique évaluée sous cycloplégie doit toujours être totale. Elle n’empêche pas toujours l’apparition d’un strabisme mais en favorise l’expression accommodative pure. Il est essentiel de prévenir à l’avance les parents que la survenue d’un tel strabisme n’est pas la conséquence de la prescription optique mais seulement le révélateur d’un état latent.
L’hérédité strabique n’étant qu’un des éléments du risque strabique, la seule présence d’une hypermétropie significative chez le nourrisson représente également un risque. La marge de manœuvre est toutefois un peu plus souple et rejoint celle de la prévention de l’amblyopie.
On rappellera tout d’abord que l’existence d’un strabisme constitue à elle seule un risque amblyopique d’environ 50 %. Néanmoins le principal risque amblyopique est lié à l’astigmatisme et à l’anisométropie (tableau 4-IV). Comme pour le strabisme, le degré d’amétropie détermine la conduite à tenir.
Le risque strabique et amblyopique est évident pour l’hypermétropie — avec 45 % de strabisme pour une hypermétropie supérieure 6,50 d —, surtout lorsque s’y associent astigmatisme et anisométropie. Dans ces conditions, la correction optique totale reste la règle. Un contrôle quatre mois plus tard permet de confirmer ou non la continuité de cet état. Dans la majorité des cas, l’hypermétropie se confirme plutôt à la hausse. Pour l’anisométropie et l’astigmatisme, c’est le risque amblyopique qui est le risque majeur, le strabisme n’étant que secondaire. La correction totale de l’amétropie s’impose également.
Le risque immédiat de pathologie est plus limité. Le bon sens conduit à une simple surveillance avec contrôle quatre mois plus tard :
-
en cas de régression de l’hypermétropie, il s’agira le plus souvent d’une emmétropisation retardée qu’il faudra vérifier à l’examen des deux ans ;
-
en l’absence d’amélioration, il paraîtra plus prudent de donner une correction subtotale.
Dans certains cas, la régression apparente de l’hypermétropie peut correspondre à un spasme accommodatif qui sera révélé secondairement par l’apparition d’un strabisme, en l’occurrence non prévisible.
La persistance d’une anisométropie est le plus souvent le signe d’un risque amblyopique. Il en est de même pour l’astigmatisme surtout s’il apparaît une régression uniquement unilatérale.
Comme pour l’application de la correction optique totale dans le strabisme avéré, le caractère préventif d’une correction précoce de la forte hypermétropie a été mis en cause à partir de protocoles de corrections partielles avec comme conclusion l’inefficacité du dépistage réfractif précoce [4, 26]. Le choix de ces sous-corrections de l’hypermétropie et de l’astigmatisme était fondé sur le même motif de respecter le processus d’emmétropisation. Même si des travaux prospectifs restent à réaliser, l’application de la correction optique totale constitue de toute évidence la meilleure mesure préventive vis-à-vis du risque strabique.
En ce qui concerne l’amblyopie, le résultat est encore plus manifeste à condition d’adjoindre à la correction optique totale les mesures de lutte contre la dominance anormale, bien connue dans le strabisme et souvent négligée dans les amétropies avec orthophorie.
En l’état actuel du dépistage systématique des troubles visuels, les examens prévus dans le cadre de la prévention maternelle et infantile se situent entre les âges de trois et six ans. Ils font suite au dépistage clinique conseillé dans le carnet de santé et qui est confié aux généralistes et aux pédiatres. Le dépistage visuel comporte entre autres la mesure de l’acuité visuelle et éventuellement un test évaluant la tolérance d’une correction hypermétropique.
Tout enfant adressé à l’ophtalmologiste pour une anomalie certaine ou suspectée doit systématiquement faire l’objet d’une réfraction cycloplégique. En l’absence de pathologie strabique ou amblyopique, la règle de la correction optique totale doit ici être modulée.
Dans le cas d’une simple baisse visuelle, il n’y a en principe pas de trouble accommodatif. Un des objectifs sera donc de laisser s’exercer la partie physiologique de l’accommodation. Cette dernière est probablement variable selon les individus, mais il existe un point de repère qui est le fait qu’à plus ou moins court terme la réfraction physiologique correspond à une hypermétropie fonctionnelle de + 0,50 d à + 0,75 d. Cette dernière évite manifestement le passage en myopie lors des fluctuations accommodatives dans les changements de fixation.
La seconde base de la démarche consiste donc à évaluer l’importance de la stimulation accommodative excessive. Celle-ci est variable en fonction de l’âge et du degré d’hypermétropie. Ainsi entre trois et six ans, le plafond physiologique de l’hypermétropie passe de + 3,00 d à + 2,25 d [12]. En principe, c’est donc au-delà de ces limites que survient le risque de fatigue et d’épuisement accommodatifs et donc une indication à la correction optique. Dans certains cas cependant, même dans les limites réfractives considérées comme physiologiques, il existe une fatigue accommodative qualifiée d’asthénie, et qui requiert une correction.
Elle va donc être graduée de façon empirique :
-
si hypermétropie < 2,00 d, la correction sera COT – 0,75 d ;
-
si hypermétropie < 3,00 d, la correction sera COT – 0,50 d ;
-
si hypermétropie < 4,75 d, la correction sera COT – 0,25 d.
Au-delà de ces valeurs, on retombe dans la zone à risque et la correction sera totale (COT).
L’acquisition d’une acuité visuelle optimale n’est réalisée qu’entre quatre et six ans. Ce constat amène à supposer qu’une myopie faible ne puisse avoir de réelle incidence au cours des premières années. En revanche, dès qu’une correction s’impose, la logique est de donner exactement la correction cycloplégique tant qu’un contrôle subjectif fiable ne peut être réalisé.
Les conséquences de l’astigmatisme sur l’acuité sont un peu plus difficiles à évaluer que dans le cadre des amétropies sphériques. La démarche de prescription suit néanmoins la même règle. L’évaluation objective de l’astigmatisme présentant une marge d’incertitude de ± 0,50 d, là encore la valeur cycloplégique sera retenue en attendant plus de précision subjective.
Dès lors qu’il existe une indication à la correction optique, celle-ci ne doit jamais comporter de sous-correction supérieure à 0,75 d en ce qui concerne l’hypermétropie. La myopie et l’astigmatisme requièrent la correction la plus exacte possible. L’habitude ancestrale de ne corriger que la moitié de l’amétropie est plus destinée au confort du praticien qu’à celui de son patient et doit être définitivement oubliée.
Dans cette période, les éventuels bilans scolaires ou les observations menées par les enseignants ou les parents amènent à identifier toute une série de signes visuels ou fonctionnels. Dans la majorité des cas, le bilan retrouve préférentiellement des myopies débutantes pour les baisses visuelles et de petits astigmatismes pour les céphalées, les clignements ou la fatigue visuelle. Néanmoins, il n’est pas exceptionnel de découvrir d’importantes hypermétropies passées inaperçues. C’est également une période privilégiée pour l’asthénie accommodative et la prescription pour quelques années d’un + 0,50 ou + 0,75 aura le plus souvent des effets bénéfiques. Globalement, les règles de prescription sont identiques à celles exposées précédemment.
Une conduite optimale de la réfraction subjective montre que la plupart des hypermétropes sont sous-corrigés dans des proportions parfois notables. La période de la presbytie en est le révélateur le plus fréquent. Si cette sous-correction est souvent bien tolérée, elle a en revanche un retentissement en nécessitant une addition progressive anormalement élevée en vision de près, ce qui est la principale source d’inconfort. En ce qui concerne la myopie, il n’est pas exceptionnel de voir apparaître des myopies tardives et des évolutions prolongées.
Chez l’enfant, la gestion des amétropies dans leur ensemble et en particulier de l’hypermétropie ne peut se concevoir qu’au travers d’examens réfractifs sous cycloplégie et de préférence répétés. La correction optique totale est requise dans toutes les situations de pathologie strabique et amblyopique, mais aussi pour toutes les hypermétropies à partir de 5,00 d. Cette règle est totalement applicable chez l’adulte. Une légère sous-correction au moins initiale est conseillée pour les amétropies moyennes. L’objectif sera de toute façon de donner la correction subjective maximale ; contrairement aux idées reçues, c’est la plus efficace et souvent la mieux tolérée. Ces différentes stratégies n’ont évidemment d’effet que dans le cadre d’une réelle coopération des patients.
[1] Angi M, De Bideran M, Bonnac J.P, Capart V et al. La réfraction. A & J Péchereau éditeurs, Nantes, 2007.
[2] Anker S, Atkinson J, Braddick OJ et al. Non-cycloplegic refractive screening can identify infants whose visual outcome at 4 years is improved by spectacle correction. Strabismus, 2004 ; 12 : 227-245.
[3] Atkinson J, Braddick OJ, Bobier B et al. Two infant vision screening programmes: prediction of strabismus and amblyopia from photo-and-video refractive screening. Eye, 1996 ; 10 : 189-198.
[4] Atkinson J, Braddick OJ, Wattam-Bell J et al. Photorefractive screening of infants and effects of refractive correction. Invest Ophthalmol Vis Sci (Suppl), 1987 ; 28 : 399.
[5] Audren F. Mise au point sur les études PEDIG. 2009. www.amblyopie.net/Documents.
[6] Auffarth G, Hunold W. Cycloplegic refraction in children: single-dose-atropinization versus three-day-atropinization. Doc Ophthalmol, 1992 ; 80 : 353-362.
[7] Birch EE, Fawcett SL, Stager DR Sr. Risk factors for development of accommodative esotropia following treatment for infantile esotropia. J AAPOS, 2002 ; 6 : 174-181.
[8] Black BC. The influence of refractive error management on the natural history and treatment outcome of accommodative esotropia. Trans Am Ophthalmol Soc, 2006 ; 104 : 303-321.
[9] Caputo A-R, Lingua RW. The problem of cycloplegia in the pediatric age group: a combination formula for refraction. J Pediatr Ophthalmol Strabismus, 1980 ; 17 : 119-128.
[10] Choong YF, Chen AH, Goh PP. A comparison of autorefraction and subjective refraction with and without cycloplegia in primary school children. Am J Ophthalmol, 2006 ; 142 : 68-74.
[11] Ciner E, Carter A, Ying GS, Maguire M, Kulp MT. Vision in Preschoolers (VIP) Study Group. Comparison of the Retinomax and Palm-AR auto-refractors : a pilot study. Optom Vis Sci, 2011 ; 88 : 830-836.
[12] Clergeau G. La réfraction de l’enfant. Cahiers de Sensorio-Motricité. A & J Péchereau éditeurs, FNRO Éditions, Nantes, 2008 ; www.larefraction.net.
[13] Clergeau G, Morvan M, Beaussac B. Bilan de 10 années de réfraction systématique sous cycloplégie chez l’enfant de 6 mois à 3 ans. Bull Soc Ophtalmol Fr, 1990 ; 6-7 : 719-726.
[14] Cordonnier M, Dramaix M. Screening for refractive errors in children: accuracy of the hand held refractor Retinomax to screen for astigmatism. Br J Ophthalmol, 1999 ; 83 : 157-161.
[15] Damanakis A. La skiascopie. A & J Péchereau éditeurs, Nantes, 2007.
[16] Denis D, Burillon C, Hadjadt E. Intérêt de la surveillance de la réfraction chez l’enfant opéré d’un strabisme congénital. Bull Soc Ophtalmol Fr, 1997 ; 97 : 379-385.
[17] Dobson V, Sebris SL, Carlson MR. Do glasses prevent emmetropization in strabismic infants? Invest Ophthalmol Vis Sci, 1986 ; 27 suppl : 2.
[18] Dufier J-L, Abitbol M, Pigamo F. Évaluation des performances d’un réfractomètre automatique sur 3 618 yeux. J Fr Ophtalmol, 1987 ; 10 : 301-308.
[19] Freeley D, Nelson L, Calhoun J. Recurrent esotropia following early successful surgical correction of congenital esotropia. J Pediatr Ophthalmol Strabismus, 1983 ; 20 : 68-71.
[20] Gadioux-Maddern F, Lelez M-L, Sellami L, et al. Influence de l’instillation de 2 ou 3 gouttes de cyclopentolate à 0,5 % sur la réfraction de l’enfant caucasien non strabique. J Fr Ophtalmol, 2008 ; 31 : 51-55.
[21] Hunold W, Auffarth G. Refraction by atropine cycloplegia. Ophthalmologica, 1991 ; 202 : 26-32.
[22] Hutcheson KA, Ellish NJ, Lambert SR. Weaning children with accommodative esotropia out of spectacles: a pilot study. Br J Ophthalmol, 2003 ; 87 : 4-7.
[23] Ingram RM, Gill LE, Goldacre MJ. Emmetropization and accommodation in hypermetropic children before they show signs of squint – A preliminary analysis. Bull Soc Belge Ophthalmol, 1994 ; 253 : 41-56.
[24] Ingram RM, Gill LE, Lambert TW. Effect of spectacles on changes of spherical hypermetropia in infants who did, and did not, have strabismus. Br J Ophthalmol, 2000 ; 84 : 324-326.
[25] Ingram RM. The problem of screening children for visual defects. Br J Ophthalmol, 1977 ; 61 : 4-7.
[26] Ingram RM. Should pre-school children be screened for visual defects? Trans Ophthalmol Soc UK, 1985 ; 104 : 646-647.
[27] Kleinstein RN, Mutti DO, Manny RE, et al. Cycloplegia in African-American children. Optom Vis Sci, 1999 ; 76 : 102-107.
[28] Lassale D, Péchereau A. Réfractomètre fixe, réfractomètre portable : une comparaison. J Fr Orthopt, 2002 ; 34.
[29] Liang CL, Hung KS, Park N, Chan P, Juo SH. Comparison of measurements of refractive errors between the hand-held Retinomax and on-table autorefractors in cyclopleged and noncyclopleged children. Am J Ophthalmol, 2003 ; 136 : 1120-1128.
[30] Mohindra I. A non cycloplegic refraction technique for infants and young children. J Am Optom Assoc, 1977 ; 48 : 518-523.
[31] Mohney BG, Lilley CC, Green-Simms AE et al. The long-term follow-up of accommodative esotropia in a population-based cohort of children. Ophthalmology, 2011 ; 118 : 581-585.
[32] Mulvihill A, McCann A, Flitcroft I et al. Outcome in refractive accommodative esotropia. Br J Ophthalmol, 2000 ; 84 : 746-749.
[33] Nirenberg N, Mazow M. The frequency and correction of accommodative esotropia following surgical correction of congenital esotropia. Binocular Vis, 1985 ; 1 : 71-76.
[34] Paff T, Oudesluys-Murphy AM, Wolterbeek R, Swart-Van den Berg M, de Nie JM, Tijssen E et al. Screening for refractive errors in children: the plusoptiX S08 and the Retinomax K-plus2 performed by a lay screener compared to cycloplegic retinoscopy. J AAPOS, 2010 ; 14 : 478-483.
[35] Péchereau A. Méthodes instrumentales de la réfraction. In : La réfraction de l’œil. Roth A, Gomez A, Péchereau A (éd.). Paris, Elsevier, 2007.
[36] Péchereau A. Le protocole pharmacologique : la cycloplégie. In : Clergeau G. La réfraction de l’enfant. Cahiers de Sensorio-Motricité. A & J Péchereau éditeurs, FNRO Éditions, Nantes, 2008 : 13-30.
[37] Prabakaran S, Dirani M, Chia A, Gazzard G, Fan Q, Leo SW et al. Cycloplegic refraction in preschool children : comparisons between the hand-held autorefractor, table-mounted autorefractor and retinoscopy. Ophthalmic Physiol Opt, 2009 ; 29 : 422-426.
[38] Quéré M-A. Emploi diagnostique et thérapeutique de la cycloplégie au cyclopentolate. Arch Ophtalmol (Paris), 1976 ; 36 : 683-688.
[39] Raab EL, Spierer A. Persisting accommodative esotropia. Arch Ophthalmol, 1986 ; 104 : 1777-1779.
[40] Repka MX, Wellish K, Wisnicki H et al. Changes in refractive error of 94 spectacle-treated patients with acquired accommodative esotropia. Binoc Vis, 1989 ; 4 : 15-21.
[41] Roth A. Anomalies réfractives, accommodation et acuité visuelle. In : La Réfraction. Cahiers de Sensorio-Motricité. A & J Péchereau éditeurs, FNRO Éditions, Nantes, 2000 : 117-123.
[42] Simonsz HJ, Eijkemans MJ. Predictive value of age, angle, and refraction on rate of reoperation and rate of spontaneous resolution in infantile esotropia. Strabismus, 2010 ; 18 : 87-97.
[43] Swan KC. Accommodative esotropia long range follow-up. Ophthalmology, 1983 ; 90 : 1141-1145.
[44] Thomas C, Caissial C. Cycloplégie induite par le cyclopentolate dans l’examen de la réfraction. Bull Soc Ophtalmol Fr, 1974 ; 5-6 : 621-631.
[45] Uretmen O, Civan BB, Kose S et al. Accommodative esotropia following surgical treatment of infantile esotropia: frequency and risk factors. Acta Ophthalmol, 2008 ; 86 : 279-283.
[46] Wary P, Maÿ F. Réfraction oculaire. Encycl Méd Chir (Elsevier, Paris), Ophtalmologie, 21-070-A-10, 2007.
[47] Wildsoet C. Active emmetropisation – Evidence for its existence and ramifications for clinical practice. Ophthalmic Physiol Optic, 1997 ; 17 : 279-290.